Министерство образования и науки Российской Федерации
Федеральное государственное бюджетное образовательное учреждение
высшего профессионального образования
Кафедра химической технологии
неметаллических материалов
и физической химии
Курсовая работа
по дисциплине аналитическая химия и ФХМА
на тему: потенциометрия
Исполнитель:
Руководитель:
Работа допущена к защите "_____" _________ 20__г. _______________
(подпись)
Работа защищена "_____" _________ 20__г. с оценкой _____________ _____________
(оценка) (подпись)
Содержание
Общая характеристика потенциометрического анализа 5
1.1 Электронообменные электроды 6
1.2 Ионоселективные электроды 7
3 Виды потенциометрического метода анализа 12
5 Потенциометрическое титрование 19
5.1 Кислотно-основное титрование 20
5.2 Комплексонометрическое титрование 21
5.3 Титрование по методу осаждения 21
5.4 Окислительно-восстановительное титрование 22
6 Измерение ЭДС электрохимических цепей 22
7 Определение нитрата в техническом образце 22
7.1 Используемое оборудование и реактивы 23
ВВедение
Электрохимические методы анализа – это совокупность методов качественного и количественного анализа, основанных на использовании электрохимических процессов, происходящих в электролитической ячейке (гальваническом элементе). Электролитическая ячейка представляет собой систему, состоящую из электродов и электролитов, контактирующих между собой. На границе раздела фаз может происходить электродная реакция между компонентами этих фаз, в результате которой электрический заряд переходит из одной фазы в другую, и на межфазной границе устанавливается потенциал. В отсутствии электрического тока (I=0) в замкнутой гальванической цепи на межфазной границе устанавливается равновесие и потенциал достигает равновесного значения. Если через ячейку проходит электрический ток (I≠0), на межфазной границе равновесие не достигается и в результате электродного процесса электроны переходят из электрода в раствор (или положительный заряд в обратном направлении).
Электрохимические методы анализа основаны на использовании зависимости электрических параметров от концентрации, природы и структуры вещества, участвующего в электродной реакции или в электрохимическом процессе переноса зарядов между электродами. Согласно рекомендациям ИЮПАК * принята следующая классификация этих методов:
- Классификация, учитывающая природу источника электрической энергии в системе. Различают две группы методов:
- Методы без наложения внешнего потенциала. Здесь источник электрической энергии – сама электрохимическая система (гальванический элемент). К таким методам относятся потенциометрические методы.
- Методы с наложением внешнего потенциала. К ним относятся: кондуктометрия, вольтамперометрия, кулонометрия, электрогравиметрия.
- Классификация по способу применения:
- Прямые методы. Измеряют аналитический сигнал как функцию концентрации раствора и по показаниям прибора находят содержание вещества в растворе (прямая потенциометрия, прямая кондуктометрия и т. д.).
- Косвенные методы – это методы титрования, в которых окончание титрования фиксируют на основании измерения электрических параметров системы (кондуктометрическое, амперометрическое титрование и т. д.).
Электрические параметры (сила тока, напряжение, сопротивление) могут служить аналитическими сигналами, если они измерены с достаточной точностью. Электрохимические методы анализа используют либо для прямых измерений, основанных на зависимости «аналитический сигнал–состав», либо для индикации конечной точки титрования в титриметрии. Электрохимические методы анализа позволяют определять концентрацию вещества в широком интервале (1÷10-9 моль/л) с достаточной точностью и воспроизводимостью, могут быть легко автоматизированы и использованы в автоматических производственных циклах.
Развитию и усовершенствованию электрохимических методов анализа способствовали успехи в области электрохимии и приборостроении. Различия между электрохимическими методами анализа в основном обусловлены природой электродов и измерительными приборами.
Подробнее остановимся на потенциометрическом методе анализа.
Общая характеристика потенциометрического анализа
Потенциометрические методы анализа известны с 90–х гг. XIX в., однако признан как аналитический метод анализа только в 20–х гг. XX в.
Данный метод, основанный на измерении электродвижущих сил (ЭДС) обратимых гальванических элементов, используют для определения содержания веществ в растворе и измерения различных физико–химических величин.
В потенциометрии обычно применяют гальванический элемент, включающий два электрода, которые могут быть погружены в один и тот же раствор (элемент без переноса) или в два различных по составу раствора, имеющих между собой жидкостной контакт (цепь с переносом).
Первый электрод – это электрод, потенциал которого зависит от активности (концентрации) определяемых ионов в растворе, называется индикаторным.
Для измерения потенциала индикаторного электрода в раствор погружают второй электрод, потенциал которого не зависит от концентрации определяемых ионов. Такой электрод называется электродом сравнения. Величину ЭДС можно рассчитать по разности потенциалов этих электродов.
Зависимость величины электродного потенциала (ЭП) от активности ионов в растворе выражается уравнением Нернста:
![]() , (1)
, (1)
где Е0 – стандартный электродный потенциал; R – универсальная газовая постоянная ( R = 8.314 Дж/моль∙К); Т – абсолютная температура; n – число электронов ( ē ), участвующих в реакции; c – концентрация, моль/дм3; f – коэффициент активности.
Так как в потенциометрии используются разбавленные растворы, где f=1 , то активность (а) заменяют на концентрацию (с). Если перейти от ln к lg, то при T = 298K (25 °С) уравнение (1.1) запишется
![]() . (2)
. (2)
В потенциометрическом методе анализа используют обратимые электроды. Токи обмена для обратимых электродов достигают несколько десятков и сотен мА/см2. Потенциал у таких электродов зависит от активности компонентов электродной реакции в соответствии с термодинамическими уравнениями. На обратимых электродах быстро устанавливается равновесие, и скачки потенциалов остаются неизменными во времени. При прохождении электрического тока скачки потенциалов не должны значительно изменяться; а после выключения тока быстро должно устанавливаться равновесие. Электроды, не удовлетворяющие этим требованиям, называются необратимыми.
В потенциометрии применяют два основных класса индикаторных электродов:
- Электроды, на межфазных границах которых протекают реакции с участием электронов, так называемые электронообменные (окислительно–восстановительные, электроды первого и второго рода);
- Электроды, на межфазных границах которых протекают ионообменные реакции. Такие электроды называют мембранными, или ионообменными, их называют также ионоселективными.
- Редокс–электроды состоят из электрохимически инертного проводника (платины, графита и т. д.), погруженного в раствор, в котором находятся окисленная и восстановленная формы потенциалопределяющего вещества. Такой инертный проводник способствует передаче электронов от восстановителя к окислителю через внешнюю цепь. Примерами таких электродов могут служить редокс-электроды с ионами в различных степенях окисления: (Pt)Sn4+, Sn2+, (Pt)Fe3+, Fe2+.
Уравнение Нернста при 298 К
 , (1.1)
, (1.1)
- Электроды первого рода – электроды, находящиеся в равновесии с катионами, одноименными с металлом, и обратимые по отношению к ним. Простейший электронообменный электрод – металлическая пластинка, погруженная в раствор или расплав электролита Zn/Zn2+; Cu/Cu2+ и т. д.
Уравнение Нернста для электрода первого рода при 298 К
![]() , (1.2)
, (1.2)
- Электроды второго рода представляют собой металлические электроды, покрытые слоем труднорастворимой соли того же металла. При погружении в раствор соли одноименного аниона его потенциал будет определяться активностью иона в растворе.
- Хлорсеребряный электрод (ХСЭ) Ag, AgCl|Cl– представляет собой серебряный проводник, покрытый твердым AgCl, который погружен в насыщенный раствор KCl.
Серебро электрохимически взаимодействует со своим ионом:
Ag+ + e– = Ag. |
Уравнение Нернста для этого процесса:
![]() , (1.3)
, (1.3)
Однако в присутствии труднорастворимого AgCl активность ионов серебра очень мала и ее трудно определить. Но активность ионов Ag+ связана с легко задаваемой в данной системе активностью ионов Cl– произведением растворимости хлорида серебра ПРAgCl:
|
откуда
|
Подставляя это выражение в (1.3)
|
и обозначив
|
получим уравнение Нернста для хлорсеребряного электрода:
![]() , (1.4)
, (1.4)
Потенциалопределяющими являются ионы хлора, а электродный процесс может быть представлен уравнением
|
- Каломельный электрод (КЭ) Hg|Hg2Cl2|Cl– – это ртуть, находящаяся в контакте с пастой из смеси ртути и каломели Hg2Cl2, которая, в свою очередь, соприкасается с насыщенным раствором KCl.
Принцип действия каломельного электрода тот же, что и хлорсеребряного.
Электродная реакция сводится к восстановлению каломели до металлической ртути:
|
Потенциал каломельного электрода определяется активностью ионов хлора:
|
Электроды второго рода обеспечивают стабильное поддержание электродных потенциалов за счет постоянно большой и неизменной концентрации анионов. Поэтому они применяются как электроды сравнения в потенциометрической ячейке.
Ионоселективным электродом (ИСЭ) называется индикаторный или измерительный электрод с относительно высокой специфичностью к отдельному иону или типу ионов.
Мембрана - основной компонент любого ИСЭ. Она разделяет внутренний раствор с постоянной концентрацией определяемого иона и исследуемый раствор. Одновременно мембрана служит средством электролитического контакта между ними. Мембрана обладает ионообменными свойствами, причем проницаемость ее к ионам разного типа различна. Таким образом, ИСЭ - это аналитические устройства, позволяющие с помощью ионочувствительной мембраны узнавать конкретный тип ионов и давать информацию об их количестве в виде электрического сигнала - потенциала, который связан с активностью (концентрацией) определяемого иона в анализируемом растворе (рис. 1).

Рисунок 1 Ионоселективные электроды
Потенциал системы, состоящей из внешнего электрода сравнения и ИСЭ, погруженных в анализируемый раствор, описывается модифицированным уравнением Нернста (уравнением Никольского-Эйзенмана):
![]() . (1.5)
. (1.5)
где const ⎯ константа, зависящая от значений стандартных потенциалов внутреннего и внешнего электродов сравнения и от природы мембраны ИСЭ;
aА – активность определяемого иона А; аВ – активность мешающего иона В; ZВ – заряд мешающего иона; К– коэффициент селективности электрода по отношению к иону В.
Коэффициент селективности - это количественная характеристика избирательности электрода. Чем меньше коэффициент селективности, тем выше избирательность электрода к ионам, для которых он предназначен. Если коэффициент селективности составляет, например, 10-3, то определяемый ион фиксируется в 1000 раз чувствительнее, чем мешающий ион. Это следует понимать таким образом, что при К=10-3 можно определять концентрацию ионов А в присутствии почти 1000-кратного избытка ионов В. Если коэффициент селективности К = 1 , то мешающие и определяемые ионы вносят одинаковый вклад в электродный потенциал.
Если коэффициент селективности больше единицы, то мешающий ион определяется предпочтительнее, чем ион, для которого предназначался электрод. Такой вариант реализуется почти у всех Са-электродов, которые к Zn++ чувствительнее в 3 раза.
В тех случаях, когда исследуемый раствор содержит мешающие ионы в очень большом количестве, предварительно понижают их концентрацию химическим осаждением, комплексообразованием или другими подобными операциями.
Имеются две группы методов определения коэффициента селективности: первая - на основе отдельных растворов, один из которых содержит только ионы А, а другой - только ионы В; вторая - определение с помощью смешанных растворов.
Ионоселективные электроды имеют следующие достоинства: они не оказывают воздействия на исследуемый раствор; портативны; пригодны как для прямых определений, так и в качестве индикаторов в титриметрии.
В зависимости от типа мембраны ионоселективные электроды можно разделить на следующие группы:
- твердые электроды - гомогенные, гетерогенные, на основе ионообменных смол, стекол, осадков, моно- и поликристаллов;
- жидкостные электроды на основе жидких ионитов хелатов – нейтральные переносчики, биологически активных веществ;
- газовые и энзимные электроды.
- Электроды с твердыми мембранами.
В таких электродах мембрана изготовлена из малорастворимого кристаллического вещества с ионным типом электрической проводимости. Конструктивно электрод представляет собой трубку диаметром около 1 см из инертного полимера (обычно поливинилхлорида), к торцу которой приклеена тонкая (~0,5 мм) мембрана. В трубку заливают внутренний раствор сравнения, в который погружают электрод сравнения.
К электродам с твердой мембраной относятся: лантанфторидный электрод (мембрана на основе монокристалла LаF3), сульфидсеребряные электроды, галогенсеребряные электроды, электроды на основе сульфидов (халькогенидов) некоторых двузарядных ионов металлов, стеклянные электроды.
Наибольшее распространение получил стеклянный электрод.
Стеклянный электрод
С помощью данного вида электродов определяют рН растворов. Их изготавливают из специального электродного стекла, в состав которого входят оксиды алюминия, натрия, калия, бора и др. Мембрана таких электродов представляет собой тонкостенный шарик (~0,1 мм) диаметром 5 – 8 мм.
Существуют стеклянные электроды которые позволяют определить концентрацию ионов Na+, K+. В основе теории стеклянного электрода лежит представление о том, что стекло - это ионообменник, который может вступать в ионообменное взаимодействие с раствором. Стекло при этом рассматривается как твердый электролит. Стекло, состоящее из окислов натрия, кальция, кремния, обладает резко выраженным специфическим сродством к ионам Н+. Вследствие этого при соприкосновении с водными растворами в поверхностном слое стекол образуется слой, в котором ионы Na+ оказываются почти полностью замещенными на ионы Н+. Поэтому мембранный электрод, изготовленный из такого стекла, обладает Н+-функцией.
Введение в состав стекла окислов бария, цезия, лантана и замена натрия на литий значительно расширяет диапазон Н+-функции стеклянного электрода. Введение же окислов алюминия и бора значительно снижают Н+-функции стеклянного электрода. Таким путем удалось создать ионселективные стеклянные электроды для ионов Na+, K+, Li+, Ag+.
Продолжительность функционирования стеклянного электрода определяется рядом факторов - состав стекла, толщина рН-чувствтельного поверхностного слоя мембраны, температура и состав раствора, в котором электрод используется. Разрушение стекла водными растворами происходит в результате сорбции воды стеклом и глубокое ее проникновение в толщу. Коррозионному действию щелочных растворов, образующихся при экстракции щелочных компонентов стекла, подвергается и горловое стекло. Кремнекислородная сетка испытывает воздействие с обеих сторон мембраны. В конце концов развиваются трещины, приводящие к нарушению функции электрода. Для защиты электрода от разрушения необходимо хранить его в воде, так как в воде происходит выщелачивание связанных ионными силами основных компонентов стекла и замена их ионами водорода, в результате чего на поверхности стекла образуется слой гидролизованного кремнезема, предохраняющий стекло от дальнейшего разрушения.
Факторы, влияющие на работу твердых мембранных электродов
Для достижения теоретических функций в электродах с твердыми мембранами необходимо, что бы все твердые соединения, входящие в фазу мембраны, находились в равновесии с анализируемом раствором. Этого не произойдет, если ионы, присутствующие в анализируемом растворе, реагируют с отдельными компонентами мембраны. Наиболее типичной реакцией, характерной для мембран, содержащих галогениды серебра, является образование мене растворимой серебряной соли. Для электрода с мембраной из смеси сульфидов серебра и меди обнаружен более сложный характер влияния, связанный с образованием новой твердой фазы. Если электрод оказался в растворе, ионы которого приводят к образованию новой твердой фазы, то вернуть электрод в прежнее состояние можно выдержав его в растворе с высокой концентрацией соответствующих ионов.
- Электроды с жидкостными мембранами.
В таких электродах жидкие мембраны, представляющие собой растворенные в органических растворителях ионообменные вещества, отделяют от анализируемого раствора гидрофобными мелкопористыми пленками, пористыми дисками или гидрофобизированными керамическими диафрагмами.
Устойчивость мембраны повышается, если органическая жидкость обладает высокой вязкостью. Низкая диэлектрическая проницаемость жидкого органического вещества способствует ассоциации ионов в фазе мембраны. Высокая селективность к определяемому иону требует большой стабильности ионного комплекса, на которую влияет растворитель. Для создания электродов с жидкими мембранами используют многие органические вещества, либо чистые, либо в соответствующем растворителе. Общее свойство всех этих соединений - способность селективно связывать некоторые небольшого размера ионы, образуя нейтральные ионогенные группы с ионами противоположного знака заряда (в жидком ионообменнике) или заряженные комплексы с нейтральными группами органической природы. Жидкие мембраны разделяют две водные фазы. На границе между мембраной и раствором происходит быстрый обмен между свободными ионами в растворе и ионами, связанными органическими группами в фазе мембраны. Селективность электрода зависит от избирательности этого ионного процесса.
В электродах с жидкими мембранами к мембранному веществу предъявляется одно требование, так как если какой-либо ион способен вообще существовать в фазе мембраны, то он в ней будет двигаться по закону диффузии, и поэтому проблема обеспечения подвижности интересующего иона в мембране сама собой разрешается. Селективность жидких мембран будет определяться ограничением внедрения посторонних ионов в поверхность мембраны. Так как жидкая фаза находится вконтакте с водными растворами, она должна быть нерастворимой в воде и иметь низкое давление паров, чтобы избежать интенсивного ее испарения. Эти требованиям могут отвечать жидкие органические вещества обладающие сравнительно большим молекулярным весом и низкими диэлектрическими проницаемостями.
Их основным недостатком является постепенное вымывание анализируемым раствором ионообменника, что сокращает срок работы электрода.
Этих трудностей удалось избежать после разработки электродов с пленочными мембранами. В таких электродах в тонкую мембрану из гидрофобного полимера (поливинилхлорида) вводят пластификатор и растворенное в нем электродоактивное вещество, вступающее в ионообменную реакцию с анализируемым ионом в растворе. В настоящее время промышленность выпускает пленочные ионоселективные электроды на катионы Na+, К+, NH4+, Са2+, Mg2+; электроды для определения общей жесткости воды; на анионы галогенидов, NCS–, NО3–. Существуют электроды и на другие ионы.
- Газовые электроды
Газовый электрод включает ионоселективный электрод и сравнительный электрод, контактирующие с небольшим объемом вспомогательного раствора, который отделен от исследуемого раствора газовой прослойкой или гидрофобной газопроницаемой мембраной.
Существует два вида газовых электродов:
Первый - ионоселективный и сравнительный электрод погружены в небольшой объем раствора определенного состава, отделенного от исследуемого раствора гидрофобной газопроницаемой мембраной. Для этого вида электродов используют два вида мембран - гомогенные, представляющие собой пленку полимера, в которой растворяется диффузионный газ, и гетерогенные, микропористые, в которых газ диффундирует фактически через воздух, заполняющий поры. В качестве мембран используют - силиконовый каучук, тефлон, полипропилен. Микропористые мембраны обладают лучшими диффузионными характеристиками по сравнению с гомогенными.
Второй тип - в нем газопроницаемая мембрана заменена газовой прослойкой. В этом электроде для удержания электролита на поверхности индикаторного электрода и создания стандартной по толщине пленки в электролит вводят ПАВ или весь раствор впитывается слоем геля.
В электроде с гидрофобной мембраной не требуется обновлять слой электролита на мембране индикаторного электрода после каждого измерения; электрод можно использовать в условиях протока; на показания электрода практически не влияют механические помехи (например, сотрясение); полимерная пленка защищает электрод от воздействия воздуха.
В электроде с газовым зазором можно изменять толщину слоя электролита, изменяя давление головки электрода на полимерную мембрану; слой электролита на индикаторном электроде очень тонок, это значительно сокращает время отклика электрода; диффузия газа в воздушной прослойке происходит гораздо быстрее, чем в мембране из полимера; из-за отсутствия прямого контакта электрода с образцом значительно возрастает срок жизни электрода.
Одним из наиболее распространенных электродов, является электрод с чувствительным элементом на аммиак. Эта электродная система включает катионоселективный электрод и гидрофобную мембрану, проницаемую для аммиака, но непроницаемую для таких ионов, как Na+, K+, NH4+. Мембрана отделяет исследуемый щелочной раствор от внутреннего раствора 0,1М NH4Cl, в который погружен стеклянный рН-электрод и хлорсеребряный электрод сравнения. Диффузия аммиака через мембрану вызывает изменение рН раствора, находящегося между мембраной и стеклянным электродом, который регистрирует это изменение рН. Электроды для определения кислорода и углекислого газа используют преимущественно в медицине.
При измерении ЭДС обратимых гальванических элементов необходим полуэлемент, потенциал которого был бы неизвестен, постоянен и не зависел бы от состава полученного раствора. Электрод удовлетворяющий этим требованиям, называют электродом сравнения. Электрод сравнения должен быть прост в изготовлении сохранять практически постоянный и воспроизводимый потенциал при прохождении небольших токов.
В качестве электрода сравнения используют стандартный водородный электрод (СВЭ) – электрод I рода – Pt(H2)/2H+. Его потенциал определяется величиной pH и при комнатной температуре равен:
E = E0 + 0,059lg[H+ ] = −0,059pH .
Стандартный водородный электрод (СВЭ) неудобен в работе, его заменяют электродами II рода – насыщенным каломельным электродом (н.к.э.) и хлорсеребряным (х.с.э.).
В зависимости от природы электродной реакции на индикаторном электроде в потенциометрических методах существуют два направления: ионометрия и редоксметрия. В обоих случаях потенциометрические методы анализа подразделяются на два вида:
- прямая потенциометрия, или ионометрия;
- потенциометрическое титрование.
Метод прямой потенциометрии основан на измерении потенциала индикаторного электрода, погруженного в исследуемый раствор, и расчете концентрации определяемых ионов согласно уравнению Нернста.
Метод достаточно прост и экспрессен. Достоинством и недостатком метода одновременно является то, что измеряемый потенциал зависит от активности. Это единственный метод прямого определения активности ионов в растворах. Но с другой стороны аналитиков чаще интересует концентрация, а пересчет активности ионов в концентрацию с применением эмпирических коэффициентов активности вызывает некоторую дополнительную погрешность. Существует вариант метода, в котором в калибровочные и анализируемые растворы вводится индифферентный электролит. Это позволяет проводить калибровку и последующий анализ в единицах концентрации.
Прямая потенциометрия обладает важными достоинствами. В процессе измерений состав анализируемого раствора не меняется. При этом, как правило, не требуется предварительного отделения определяемого вещества. Метод можно легко автоматизировать, что позволяет использовать его для непрерывного контроля технологических процессов.
Исторически первыми методами прямой потенциометрии были способы определения водородного показателя (рН– метрия).
Для определения величины pH существуют два основных метода: колориметрический и потенциометрический.
Потенциометрический метод намного точнее, чем колориметрический, но требует оборудования лабораторий специальными приборами – pH–метрами.
pH-метр — прибор для измерения водородного показателя (показателя pH), характеризующего концентрацию ионов водорода в растворах, питьевой воде, пищевой продукции и сырье, объектах окружающей среды и производственных системах непрерывного контроля технологических процессов, в том числе в агрессивных средах.
Действие pH-метра основано на измерении величины ЭДС электродной системы, которая пропорциональна активности ионов водорода в растворе — pH (водородному показателю). Измерительная схема по сути представляет собой вольтметр, проградуированный непосредственно в единицах pH для конкретной электродной системы (обычно измерительный электрод — стеклянный, вспомогательный — хлоросеребряный).
Входное сопротивление прибора должно быть очень высоким — входной ток не более 10-10А (у хороших приборов менее 10-12А), сопротивление изоляции между входами не менее 1011Ом, что обусловлено высоким внутренним сопротивлением зонда — стеклянного электрода. Это основное требование к входной схеме прибора.

Наибольшее практическое применение определения величины pH нашел стеклянный индикаторный электрод, который можно использовать в широком диапазоне pH и в присутствии окислителей.
Крупный вклад в теорию и практику рН-метрии внесли ученые: Б.П. Никольский, М.М. Шульц, Е.Н. Виноградова и др.
С середины 60-х годов за рубежом, а с 70-х годов в нашей стране стала бурно развиваться новая область физико-химических методов анализа – ионометрия (рХ-метрии). Этот метод основан на разработке, изучении и практическом использовании различного рода ионоселективных электродов (ИСЭ). Иногда рН-метрию рассматривают как частный случай ионометрии. Градуировка шкал приборов потенциометров по значениям рХ затруднена из-за отсутствия соответствующих стандартов. Поэтому при использовании ионоселективных электродов активности (концентрации) ионов определяют, как правило, с помощью градуировочного графика или методом добавок. Применение таких электродов в неводных растворах ограничено из-за неустойчивости их корпуса и мембраны к действию органических растворителей.
- Метод градуировочного графика
Метод градуировочного графика является самым простым ионометрическои методом анализа. Процедура анализа состоит из 2-х этапов и включает в себя градуировку ионоселективного электрода (ИСЭ) относительно электрода сравнения и проведения измерений в пробах.
- Градуировка состоит в измерении потенциала ИСЭ в стандартных растворах с известным содержанием определяемого иона. По результатам измерений строится график. В ионометрии принято выражать концентрацию ионов через величину рХ, которая равна
pX = -lg a.
где а - активность компонента электрохимической реакции.
Поэтому из уравнения Нернста следует, что закономерность изменения потенциала имеет следующий вид:
E = B - S∙pX,
где E - разность потенциалов между ИСЭ и электродом сравнения; S - наклон электродной функции; В - константа.
Эта закономерность называется электродной функцией. В координатах Е от рХ градуировка электродов имеет вид прямой, наклон которой приближается к величине 59,2 мВ (для температуры 25 0C) для однозарядных ионов. Для двухзарядных ионов наклон равен 29,6 мВ. Если полученная из градуировки величина наклона существенно отличается от ожидаемой, то это говорит о неблагополучном ходе измерений.
- Анализ состоит в измерении потенциала ИСЭ в пробе и вычисления содержания определяемого компонента по градуировочному графику. Поскольку градуировочный график представляет собой прямую, то произвести расчеты по найденному потенциалу несложно.
На практике калибровка линейна только в определенном диапазоне концентраций. Вне этого диапазона калибровка нелинейна. В некоторых случаях можно использовать нелинейную часть калибровки, но это надо делать с оглядкой, так как не всегда можно контролировать процессы происходящие с ионоселективными электродами в этих диапазонах.
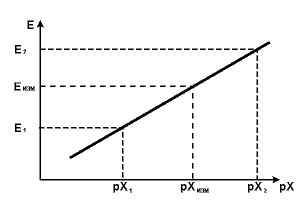
Рисунок 2 Грдуировочный график для определения концентрации методом прямой потенциометрии
Важной особенностью метода градуировочного графика является необходимость постоянства условий проведения калибровки и измерений. При проведении измерений следует, прежде всего, уделять внимание уравниванию температуры и ионной силы, как в стандартных растворах, так и в анализируемых пробах. Несоблюдение этого условия ведет к увеличению погрешности измерений
- Метод добавок
Метод добавок в ионометрии играет значительную роль. Ионометрический метод добавок дает два больших преимущества. Во-первых, если колебание ионной силы в анализируемых пробах непредсказуемо, то применение распространенного метода градуировочного графика дает большие ошибки определения. Применение метода добавок радикально меняет ситуацию и помогает свести к минимуму ошибку определения. Во-вторых, есть категория электродов, использование которых проблематично из-за дрейфа потенциала. При умеренном дрейфе потенциала метод добавок существенно снижает ошибку определения.
Существуют следующие модификации метода добавок:
- метод стандартной добавки;
- метод двойной стандартной добавки;
- метод Грана.
Все эти методы могут быть сортированы на две категории по явному математическому признаку, определяющему точность получаемых результатов. Он заключается в том, что одни методы добавок обязательно используют в расчетах предварительно измеренное значение наклона электродной функции, а другие - нет. В соответствии с этим делением метод стандартной добавки и метод Грана попадает в одну категорию, а метод двойной стандартной добавки - в другую.
Метод стандартной добавки и метод Грана
Перед тем, как излагать индивидуальные особенности той или иной разновидности метода добавок, опишем в нескольких словах процедуру анализа. Процедура состоит в том, что в анализируемую пробу делается добавка раствора, содержащего тот же анализируемый ион. После каждой добавки записываются показания электродов. В зависимости от того, как далее будут обрабатываться результаты измерений, метод будет называться методом стандартной добавки или методом Грана.
- Расчет для метода стандартной добавки выглядит следующим образом:
Cx = ΔC ( 10ΔE/S - 1)-1 ,
где Cx - искомая концентрация; ΔC - величина добавки; ΔE - отклик потенциала на введение добавки ΔC; S - наклон электродной функции.
- Расчет методом Грана выглядит несколько сложнее. Он состоит в построении графика в координатах (W+V) 10 E/S от V, где V - объем вводимых добавок; E - значения потенциала, соответствующее вводимым добавкам V; W - начальный объем пробы.
График представляет собой прямую, пересекающуюся с осью абсцисс. Точка пересечения соответствует объему вводимой добавки (ΔV), которая эквивалентна искомой концентрации иона (см. рис. 3). Из закона эквивалентов следует, что Cx = Cст ΔV / W, где Cст - концентрация ионов в растворе, который используется для введения добавок. Добавок может быть несколько, что естественно улучшает точность определения по сравнению с методом стандартной добавки.

Рисунок 3
Не составляет труда заметить, что в обоих случаях фигурирует наклон электродной функции S. Из этого следует, что первым этапом метода добавок является калибровка электродов для последующего определения величины наклона. Абсолютное значение потенциала в расчетах не участвует, так как для получения достоверных результатов важно только постоянство наклона калибровочной функции от пробы к пробе.
В качестве добавляемого можно применять не только раствор, содержащий потенциалопределяющий ион, но и раствор вещества, связывающего определяемый ион пробы в недиссоциирующее соединение. Процедура анализа при этом принципиально не меняется. Тем не менее, для этого случая существуют некоторые характерные особенности, которые следует учитывать. Особенности заключаются в том, что график экспериментальных результатов состоит из трех частей, как показано на рис.4.

Рисунок 4
Первая часть (A) получается в условиях, когда концентрация связывающего вещества меньше концентрации потенциалопределяющего. Следующая часть графика (B) получается при примерно эквивалентном соотношении вышеупомянутых веществ. И, наконец, третья часть графика (C) отвечает таким условиям, при которых количество связывающего вещества больше, чем потенциалопределяющего. Линейная экстраполяция части A графика на ось абсцисс дает величину ΔV. Область B обычно для аналитических определений не используется.
Если кривая титрования центральносимметрична, то для получения результатов анализа можно использовать и область C. Однако, в этом случае ордината должна вычисляться следующим образом: (W+V)10 -E/S .
Метод Грана обладает большими преимуществами, чем метод стандартных добавок.
Преимущества применения данных методов:
1. Уменьшение погрешности определения в 2-3 раза за счет увеличения числа измерений в одной пробе.
2. Метод добавок не требует тщательной стабилизации ионной силы в анализируемой пробе, так как ее колебания отражаются на величине абсолютного значения потенциала в большей степени, чем на величине наклона электродной функции. В связи с этим погрешность определения по сравнению с методом градуировочного графика уменьшается.
3. Применение целого ряда электродов проблематично, так как наличие недостаточно стабильного потенциала требует частого проведения процедуры градуировки. Поскольку в большинстве случаев дрейф потенциала мало сказывается на наклоне калибровочной функции, то получение результатов методом стандартных добавок и методом Грана существенно повышает точность и упрощает процедуру анализа.
4. Метод стандартных добавок позволяет контролировать правильность проведения каждого аналитического определения. Контроль производится во время обработки экспериментальных данных. Так как в математической обработке принимает участие несколько экспериментальных точек, то проведение через них прямой каждый раз подтверждает то, что математический вид и величина наклона калибровочной функции не изменились. В противном случае линейный вид графика не гарантирован. Таким образом, возможность контроля правильности анализа в каждом определении повышает надежность получения результатов.
Как уже отмечалось, метод стандартных добавок позволяет проводить определения в 2-3 раза точнее, чем метод градуировочного графика. Но для получения такой точности определения следует пользоваться одним правилом. Чрезмерно большие или малые добавки снижают точность определения. Оптимальная величина добавки должна быть такой, чтобы она вызывала отклик потенциала в 10-20 мВ для однозарядного иона. Это правило оптимизируют случайную погрешность анализа, однако в тех условиях, в которых часто применяется метод добавок, становится значимой систематическая погрешность, связанная с изменением характеристик ионоселективных электродов. Систематическую погрешность в этом случае полностью определяет погрешность от изменения наклона электродной функции. Если в течение эксперимента изменился наклон, то при определенных условиях относительная погрешность определения будет приблизительно равна относительной погрешности от изменения наклона.
Метод двойной стандартной добавки
Метод заключается в том, что к анализируемому раствору добавляются 2 порции стандартного раствора. Величина этих порций одинакова. По результатам измерений вычисляется параметр
R = ΔE2 / Δ E1 ,
где Δ E1 - разность между потенциалом электродов в анализируемом растворе, и в растворе после первой добавки; ΔE2 - разность между потенциалом электродов в анализируемом растворе, и в растворе после второй добавки.
Пользуясь вычисленным параметром, по специальной таблице находится искомое значение концентрации. Использование таблицы оправдано тем, что для поиска значения концентрации приходится решать трансцендентное уравнение R = lg(1/(1+ 2ΔV/W) + 2ΔC/Cx) / lg(1/(1+ΔV/W) + ΔC/Cx) .
Следует уточнить, что ΔС - концентрация в анализируемом растворе после добавки, если бы в этом растворе не было бы больше никаких ионов, т.е. ΔС = Сисх ΔV / (W+ ΔV). Сисх - концентрация в стандартном растворе.
В изложенных выше формулах отсутствует упоминание о наклоне электродной функции, так как это было целью разработки метода двойной стандартной добавки. На первый взгляд это факт выгодно отличает этот метод, поскольку процедура анализа упрощается, но это не так. Выиграв в одном, мы, безусловно, теряем в другом. Во-первых, для того, чтобы ошибка анализа была удовлетворительной, нужно быть уверенным в линейности электродной функции ионоселективного электрода! Отклонения от линейности будут приводить к очень большой ошибке анализа. Таким образом калибровать электроды все равно придется. Во-вторых, случайная погрешность анализа существенно больше, чем в методе Грана и методе стандартной добавки. Например, ошибка измерения потенциала в 1мВ может приводить к погрешности анализа в 10-20%.
Метод двойной стандартной добавки лучше применять только для очень надежных в эксплуатации электродов (фторидселективный).
К прямой потенциометрии относится также редоксметрия.
Редоксметрия – группа методов, в которых характеристическим свойством определяемых веществ является их способность к химическим превращениям, связанным с переносом электронов, а в качестве аналитического сигнала измеряют редокс–потенциал определяемых веществ.
Окислительно-восстановительный потенциал зависит от активностей окисленной и восстановленной форм вещества. Редоксметрию применяют также для определения концентрации ионов в растворах.
Более распространены методы потенциометрического титрования. В потенциометрическом титровании измеряют потенциал индикаторного электрода для отслеживания изменения концентрации определяемого иона в процессе химической реакции между определяемым ионом и подходящим реагентом (титрантом).
Аппаратура для потенциометрического титрования та же самая, что и для прямой потенциометрии. В схему потенциометрических измерений входят индикаторный электрод, электрод сравнения и потенциало–измеряющий прибор.
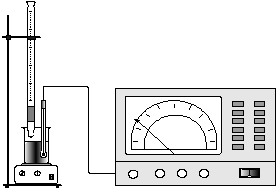
Рисунок 5 Установка для потенциометрического титрования
В ходе титрования измеряют и записывают ЭДС ячейки после добавления каждой порции титранта. В начале титрант добавляют небольшими порциями, при приближении к конечной точке (резкое изменение потенциала при добавлении небольшой порции реагента) порции уменьшают.
Для определения конечной точки потенциометрического титрования можно использовать различные способы. Наиболее простой способ состоит в построении кривой титрования –графика зависимости потенциала электрода от объема титранта (рис. 6, А). Другой способ состоит в расчете изменения потенциала на единицу изменения объема реагента ΔE/ΔV (рис 6, Б).


Рисунок 6 Кривые потенциометрического титрования
А – интегральная кривая; Б – дифференциальная кривая
При потенциометрическом титровании могут быть использованы следующие типы химических реакций, в ходе которых изменяется концентрация потенциалопределяющих ионов:
- реакции кислотно-основного взаимодействия;
- комплексообразования;
- реакции осаждения;
- реакции окисления-восстановления.
В кислотно-основном титровании в качестве индикаторного обычно используют стеклянный электрод, как правило, входящий в комплект серийно выпускаемых промышленностью pH-метров. Потенциометрический метод позволяет провести количественное определение компонентов в смеси кислот, если константы диссоциации различаются не менее чем на три порядка. Например, при титровании смеси, содержащей хлороводородную (HCl) и уксусную кислоты, на кривой титрования обнаруживается два скачка. Первый свидетельствует об окончании титрования HCl, второй скачок наблюдается при оттитровывании уксусной кислоты. Также несколько скачков имеют кривые титрования многоосновных кислот, константы диссоциации которых существенно различаются (хромовая, фосфорная и др.).
Широкие возможности анализа многокомпонентных смесей без разделения открывает применение неводных растворителей. Например, определение содержания хлороводородной и монохлоруксусной кислот в смеси титрованием водного раствора является сложной задачей в связи с трудностью обнаружения двух скачков титрования. При титровании в ацетоне оба скачка выражены достаточно четко и содержание каждой кислоты в смеси может быть рассчитано.
Потенциометрическое титрование катионов комплексоном III (ЭДТА) можно проводить с использованием в качестве индикаторного электрода соответствующего металла: титрование солей меди с медным электродом, солей цинка с цинковым и т.д. или подходящего ионоселективного электрода. Однако, многие металлические индикаторные электроды необратимы, а число ионоселективных электродов невелико.
Для комплексонометрических титрований может быть использован универсальный электрод Hg|HgY2- или Au(Hg)|HgY2-, где Au(Hg) - амальгамированное золото; HgY2- - комплекс ртути с анионом этилендиаминтетрауксусной кислоты. С помощью ртутного электрода этого типа могут быть оттитрованы любые ионы, которые образуют с Y4- комплексы с константой устойчивости, не превышающей константу устойчивости ртутного комплекса. Это, например, ионы магния (Mg2+), кальция (Ca2+), кобальта (Co2+), никеля (Ni2+), меди (Cu2+), цинка (Zn2+) и др.
Индикаторными электродами в методах потенциометрического титрования, использующих реакции осаждения, служат металлические или мембранные электроды, чувствительные к определяемому иону или иону-осадителю. Практически по методу осаждения могут быть определены катионы серебра, ртути, цинка, свинца, анионы хлора, брома, иода и некоторые другие. Смесь галогенидов, например I- и Cl-, может быть оттитрована без разделения нитратом серебра. Серебряный электрод позволяет фиксировать два скачка в ходе такого титрования. Первый скачок свидетельствует об оттитровывании иодид-иона и может быть использован для расчета содержания этого иона, второй скачок относится к окончанию осаждения хлорид-иона. По второму скачку можно рассчитать суммарное содержание галогенидов или концентрацию хлорид-иона, если концентрация иодид-иона будет известна из данных по титрованию до первого скачка.
Кривые окислительно-восстановительного титрования могут быть построены в координатах или pM - V (титранта) или E - V (титранта), если pM=-lg[M] ([M] - концентрация участника реакции, E - потенциал системы, V (титранта) - объем титранта). Кривые титрования первого типа представляют практический интерес, когда имеется индикаторный электрод, чувствительный к M. Кривые второго типа имеют более общее значение, так как любое окислительно-восстановительное титрование может быть проведено по измерению E с использованием индикаторного электрода из благородного металла, чаще всего платины.
Результаты определения методом потенциометрического титрования более точны, чем при использовании прямой потенциометрии, так как в этом случае вблизи точки эквивалентности небольшому изменению концентрации соответствует большое изменение потенциала индикаторного электрода.
К недостаткам потенциометрического титрования можно отнести не всегда быстрое установление потенциала после добавления титранта и необходимость во многих случаях проводить при титровании большое количество отсчетов.
Его возможности существенно расширились с разработкой новых ионоселективных электродов как индикаторных. Метод применяют при анализе мутных, загрязненных и окрашенных растворов в смешанных и неводных растворителях.
При измерении ЭДС электрохимических цепей, применяемых в потенциометрии, необходимо снимать ничтожно малые токи (10–13 – 10–14 А ), чтобы не вызвать поляризацию электродов. Это возможно лишь при использовании компенсационного способа измерения ЭДС. В настоящее время промышленность выпускает для этих целей специальные приборы: рН – метры и иономеры, позволяющие измерять ЭДС в интервале ± 1900 мВ. Наиболее распространенными являются иономер ЭВ–74 со стрелочной индикацией, а также иономеры И –130 и И –140 с цифровой индикацией. На этих приборах возможно измерение не только ЭДС, но и рН или рХ растворов, где Х – катион или анион, к которому селективен применяемый ионоселективный электрод.
Как правило, определение нитрата в технических объектах является сложной аналитической задачей, на выполнение которой затрачивается большое количество времени. Применение ионоселективных пластифицированных электродов, чувствительным элементом которых является мембрана, содержащая нитратную соль четвертичного аммониевого основания, позволяет быстро решить поставленную задачу.
- рН–Метр, рН–121 или иономер ЭВ–74.
- Нитратселективный пластифицированный электрод.
- Хлорсеребрянный электрод сравнения.
- Магнитная мешалка.
- Мерные колбы вместительностью 100 мл.
- Пипетка вместительностью 10 мл.
- Стаканы вместительностью 50 мл.
- Нитрат калия.
- Сульфат калия, 1 М раствор.
- Технические образцы селитры с содержанием нитрата до 60%.
По точной навеске методом разбавления готовят серию стандартных растворов нитрата калия (10-1–10—5). Так как нитратселективный электрод реагирует на изменение активности ионов нитрата, а не концентрации, то более правильно готовить растворы с постоянной ионной силы, создаваемой 1 М раствором сульфата калия. В этом случае стандартные растворы KNO3 готовят на фоне 1 М раствора K2SO4. Исследуемый раствор также готовят на фоне сульфата калия. Погружают электроды в анализируемый раствор и регистрируют зависимость ЭДС элемента, составленного из нитратселективного электрода и электрода сравнения, от концентрации нитрата калия. Строят калибровочный график зависимости Е=f(–lgc). Перед началом измерений необходимо несколько раз тщательно промыть электроды дистиллированной водой. При использовании стандартных растворов измерения необходимо проводить, переходя от разбавленных к концентрированным растворам.
Навеску технического образца, в котором необходимо определить содержание нитрата (≈0,1000 г), взвешенную на аналитических весах. Переносят в мерную колбу вместительностью 100 мл и доливают до метки дистиллированную воду. Измеряют ЭДС элемента в исследуемом растворе.
Используя калибровочный график, определяют содержание нитрата в анализируемом растворе. Содержание нитрата x (в %) в техническом образце рассчитывают по формуле: ![]() ,
,
где с – концентрация NO3-, определяемая из графика, моль/л; V – вместимость мерной колбы; М – молекулярная масса нитрата; g – навеска технического образца, г.
Описанная методика может быть использована для определения содержания фторидов и хлоридов с помощью фторид– и хлоридселективных электродов соответственно. Для создания постоянной ионной силы целесообразно использовать ацетатный буферный раствор (при определении).
Заключение
Главное преимущество потенциометрического метода по сравнению с другими методами анализа – быстрота и простота проведения измерений. Время установления равновесного потенциала индикаторных электродов мало, что удобно для изучения кинетики реакций и автоматического контроля технологических процессов. Используя микроэлектроды, можно проводить определения в пробах объемом до десятых долей, см3. Потенциометрический метод дает возможность проводить определения в мутных и окрашенных растворах, вязких пастах, при этом исключая операции фильтрации и перегонки. Потенциометрические измерения относят к группе неразрушающих способов контроля, и анализируемый раствор может быть использован для дальнейших исследований. Погрешность определения при прямом потенциометрическом измерении составляет 2 – 10 %, при проведении потенциометрического титрования – 0,5 – 1,0 %. Интервал определения содержания компонентов потенциометрическим методом в различных природных и промышленных объектах – в пределах от 0 до 14 рН для стеклянных электродов, и от 10 до 10–5(10–7) М определяемого иона для других типов ионоселективных электродов.
Одним из достоинств метода потенциометрического титрования является возможность полной или частичной его автоматизации. Автоматизировать можно подачу титранта, запись кривой титрования, отключение подачи титранта в заданный момент титрования, соответствующий точке эквивалентности.
Библиографический список
- Лебедева М.И. Аналитическая химия и физико-химические методы анализа – Тамбов : Изд-во Тамб. гос. техн. ун-та, 2005. 216 с.
- Васильев В.П. Аналитическая химия. Ч.2. – М.: Высш. шк., 2002.–350с.
- Практикум по физико-химическим методам анализа. Под редакцией Петрухина О.М. – М. :Химия, 1987
- Агасян П. К., Николаева Е. Р., Основы электрохимических методов анализа (потенциометрический метод), М., 1986.
- Никольский Б.П., Матерова Е.А. "Ионоселективные электроды" -Л.: Химия, 1980.-240 с.

